Det stigende indhold af CO2 i atmosfæren og vores fortsatte udledninger har medført et større indhold af CO2 i havvandet. CO2 virker som en syre, og derfor er havet blevet ”forsuret” i den anledning. Surheden måler man efter den såkaldte pH-skala, der går fra 1 til 14, hvor 1 er stærkt sur, og 14 er det stik modsatte, stærkt basisk.
Surhed er udtryk for antallet af brint-ioner (H+) i vandet. pH-skalaen er såkaldt logaritmisk, således at ved pH = 2 er der 10 gange så mange brint-ioner som ved pH = 3 og 100 gange så mange som ved pH = 4 og sådan fremdeles.
Destilleret vand, som hverken er surt eller basisk, har pH = 7. Det kalder man ”neutralt”. Der er stadigvæk en lille smule brint-ioner tilbage her, og ved pH = 8 er der så igen kun en tiendedel af dette antal.
Mange af de væsker, vi drikker, er faktisk ret sure, således har cola en pH på 2,5, mens æblejuice har pH = 3,5.
Havvand har typisk en pH omkring 8, dvs. det er basisk. I praksis kan pH dér kortsigtet svinge mellem 7,5 og 8,5, det afhænger af havstrømmene, især når vand fra dybere liggende lag bliver sendt op til overfladen og vice versa.
Det menes nu, at vores CO2-udledninger har medført et fald i havenes gennemsnitlige pH fra 8,12 til 8,07. Det er ikke nogen nem måling at foretage, men selvom tallene skulle være korrekte, må det selvfølgeligt slås fast, at der ikke i den forbindelse er tale om nogen ”forsuring”. Havvandet er stadigvæk solidt i det basiske område, og langt inden for de naturlige variationer, der opleves lokalt.
Nu hævdes det i flere klima-alarmistiske tekster, at ”forsuringen” allerede nu medfører at muslinger og andre skaldyr går i opløsning pga. faldet i pH.
Muslingeskaller er opbygget af kalk, også kendt som calciumkarbonat, CaCO3. Når vi afkalker hjemme i badeværelset, bruger vi et produkt, der indeholder syre, og syren angriber kalken og nedbryder den. Vi ser, at det bruser op fra stedet. Den kemiske reaktion ser således ud (men den er ikke afgørende for forståelsen her):
CaCO3 + 2H+ → Ca++ + CO2 + H2O
Det, der bruser, er CO2-en, der frigøres. Derudover dannes der vand.
Nu har vi jo set, at selv ved pH 8 er der en lille smule brint-ioner til stede. Det er der også ved højere pH-værdier. Så hvorfor nedbrydes kalkskallerne så ikke – bare lidt?
Det er der flere grunde til, men en af dem er, at kalken i skallerne slet ikke er i direkte kontakt med havvandet. Muslingen har nemlig opbygget et ganske tyndt lag uden på skallens overflade, en slags hud. Og den kan sagtens modstå langt lavere pH-værdier – også under pH 7. Der findes jo også skaldyr i ferskvandssøer og -floder og her kan pH ofte være nede omkring 6. Det er ikke noget problem.
Det bliver nu interessant at se, hvordan muslingen overhovedet opbygger sin skal. Den skal bruge calcium, CO2 og vand til formålet. Faktisk er det processen ovenfor, bare omvendt:
Ca++ + CO2 + H2O → CaCO3 + 2H+
Så ligesom planterne er afhængige af, at der er CO2 omkring dem, så kan skaldyrene heller ikke leve, hvis ikke de har adgang til CO2. For 530 millioner år siden oplevede Jorden det, man kalder den ”Kambriske eksplosion”, hvor der ude i havet opstod en lang række nye arter og grupper af dyr, herunder mange skaldyr. Den gang var der 5000 ppm CO2 i atmosfæren, og der har været tilsvarende store mængder i havet. De bragte ikke skaldyrene i fare, tværtimod, de var nok en af hovedårsagerne til, at livet udviklede sig så hurtigt, som det gjorde.

For nu lige at nørde lidt mere. Vi kan se, at kalk i grunden består af to ioner, calcium- og karbonat-ionen:
Ca++ + CO32– → CaCO3
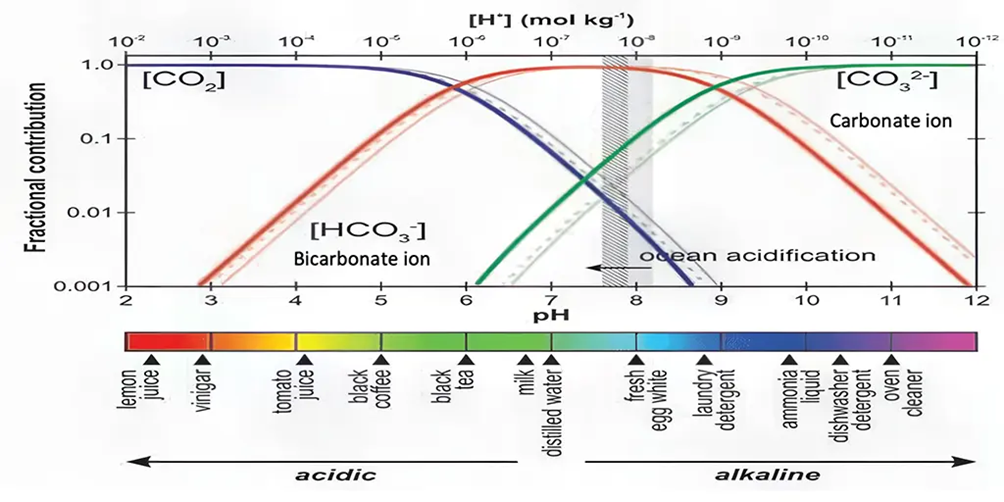
Så muslingen skal bare have fat i de to, så kan den producere kalk. Men, som vist på fig. 1, så er der ikke ret mange karbonat-ioner tilstede ved den pH, vi har i havet, måske kun 5 % af kulstoffet findes som karbonat-ioner. Der er endnu mindre CO2, langt under 1%. Langt det meste er omdannet til en mellemform, HCO3– også kendt som bikarbonat. Og det viser sig, at det netop er denne mellemform, skaldyret henter ind, når det skal bygge på sin skal. Men for at kunne bruge bikarbonat-ionen skal dens ene brintatom skilles fra, det bliver som en brint-ion og derved falder pH drastisk lige der, hvor processen foregår. Alt det har muslingen naturligvis fuldt styr på. Faktisk viser det sig, at den aldrig bruger CO2, når den skal bygge skal, men derimod bikarbonat-ioner.
Og hvad kan vi så konkludere om forsuringen, der ofte bliver brugt som et vigtigt argument mod fortsatte udledninger af CO2?
For det første er der ikke tale om nogen forsuring, havets pH forbliver langt over 7, uanset hvor meget CO2 vi kunne finde på at udlede.
For det andet er skaldyrene slet ikke truet af de ændringer i havets pH, der kunne blive tale om. Skallerne er beskyttet mod lavere pH og dyrenes interne processer til dannelse af kalkskaller foregår under alle omstændigheder ved lavere pH end det omgivende havs.
Så forsuring er en politisk opfindelse, et led i klimakampen og slet ikke noget reelt problem.








Fremragende artikel. Tak. Hvis jeg underviste i kemi, samfundsfag eller dansk eller andet sprog, ville jeg give mine elever teksten. I sprogfag kan eleverne oversætte teksten.
Kun en kvantitativ beregning i ligevægts-reaktionsligningen nedenfor kan vise, i vor høj grad den lavere opløselighed af CO2 i vand ved 2 grader højere havvands-temperatur kompenserer for den højere opløselighed af CO2 i vand ved 300 ppm stigning af CO2 i atmosfæren:
CaCO3 + CO2 + H2O Ca(HCO3)2
Min skøn som gammel kemiker-nørd uden at have regnet efter er, at nævnte ændring ikke kan øge opløseligheden af CaCO3 mærkbart.
Jeg vil i øvrig komplimentere Søren for kvaliteten af hans argumentation. En kvalitet, man sjældent ser i klimaalarmisternes argumentation.
Man skal vel også tage hensyn til, at ved stigende temperatur falder opløseligheden af gassen CO2 i havvandet, så CO2 damper af i takt med, at havvandet bliver varmere! Imidlertid betyder det varmere vand en øget hastighed af dissociation af “kulsyren”, som skaber lavere pH i havvandet. Desuden er der en “kulsyre” puffer, som stabiliserer det komplekse ligevægtssystem, hvor Le Chateliers princip gælder. Hertil kommer interaktioner med andre stoffer opløst i havvandet. Virkeligheden er mere kompliceret end mange tror!
Én mands himmerig’ – en anden mands helved’.