Elektrolyse af vand til brint og ilt har været kendt i mere end 200 år. I princippet skal man stikke to elektroder ned i en kop vand og sætte strøm til. Brint vil da boble op ved den ene elektrode og ilt ved den anden, man har således adskilt vandet i sine bestanddele, brint og ilt.
Ilten har begrænset anvendelse, hvorimod brint allerede i dag bruges i enorme mængder, bl.a. i forbindelse med olieraffinering, hvor tunge olier kan omdannes til lettere ved tilsætning af brint. Brint er også den ene komponent til ammoniakproduktion, hvor brinten føres sammen med luftens kvælstof.
Brint fremstilles i dag enten på basis af naturgas, metan, der jo indeholder masser af brint, eller også ud fra kul og vanddamp, den gamle bygas-produktion hvor kul + vanddamp ved høje temperaturer bliver til kulmonoxid og brint.
Elektrolyse har hele tiden været en dyrere metode pga. det store forbrug af elektricitet. Kun på steder, hvor strømmen reelt var næsten gratis, har processen været rentabel.
Som et led i den grønne omstilling er interessen for brintfremstilling ved elektrolyse imidlertid eksploderet. I fremtiden vil vi have uanede mængder af strøm til rådighed fra vindmøller og solceller, og en stor del skal bruges til fremstilling af brændstoffer til de anvendelser, som man ikke så godt kan elektrificere, f.eks. tung vejtransport, flyvning, skibsfart og visse industriprocesser. Disse brændstoffer går under fællesbetegnelsen Power to X.
Første trin ved enhver Power to X proces er altid fremstilling af brint ved elektrolyse. I det følgende vil vi gennemgå de 3 mest brugte – eller lovende – teknologier og se på fremtidsmulighederne.
Alkalisk elektrolyse
Den alkaliske elektrolyse er den traditionelle fremgangsmåde. Fig. 1 viser en illustration af processen. Ved den ene elektrode, katoden, skilles vandet ad i brintioner (H+) og hydroxid-ioner (OH–). Katoden leverer den manglende elektron til brintionen, der bliver til fri brint, der derefter bobler ud af karret. Ved anoden bliver der trukket elektroner ud, og 2 hydroxid-ioner omdannes til vand og fri ilt. De to halvdele af cellen er adskilt af en membran, dvs. en væg, der tillader at OH–-ioner vandrer igennem, hvorimod brint ikke kan vandre den anden vej. Dette er vigtigt, for ellers får man ikke de rene gasser ud, og en forurening af ilten med bare lidt brint kan give en ubehagelig eksplosiv blanding.
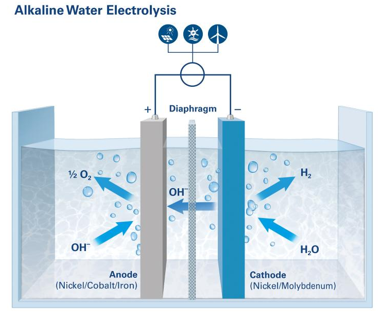
Vandet skal være rent for at undgå sidereaktioner, men man er nødt til at tilsætte et basisk stof, f.eks. kaliumhydroxid, KOH for at få vandet til at lede strømmen. Havvand leder også strømmen godt, men det går slet ikke til elektrolyse, fordi så får man uddrivning af klorgas ved den ene elektrode (anoden).
Alkalisk elektrolyse foregår ved en relativt lav temperatur, 60-80 grader og almindeligt atmosfæretryk. Man har dog eksperimenteret med højere temperaturer og tryk, sidstnævnte kommer vi tilbage til senere.
Udbyttet af energien, dvs. energiindholdet af brinten sammenholdt med den brugte mængde strøm, ligger p.t. omkring 70 %, men der er forhåbninger om, at effektiviteten kan bringes op i nærheden af 80 %, hvilket nok er den maksimale grænse.
Alkaliske elektrolyse-anlæg er pladskrævende, men til gengæld fordrer de ikke dyre metaller til elektroder eller membraner. De er derfor billigst i investering og vedligehold. De har den ulempe, at de er relativt længe om at starte op, det vil tage op til 50 minutter.
PEM elektrolyse
PEM står for Proton Exchange Membrane ”Proton-udvekslings-membran”. P-et står nogle gange for ”Polymer” i stedet for ”Proton”. Her er det brintionen (protonen), der vandrer igennem membranen i midten, se fig. 2.
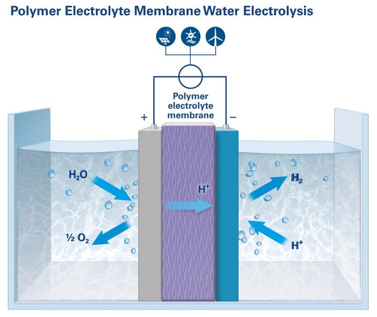
Udformningen er mere kompakt end den alkaliske elektrolyse-celle og det er lettere at sikre en høj renhed af brinten og ilten. Til gengæld skal man bruge syre i vandet, og det betyder at elektroderne skal fremstilles af ædelmetaller (platin eller iridium), der er meget mere kostbare og har kortere levetid.
PEM kører fint ved temperaturer under 100 grader og atmosfæretryk, men kan også arbejde under højere tryk. Effektiviteten er omtrent som for den alkaliske celle, dvs. omkring 70 %, med udsigt til måske 80 % (maks.).
PEM har den fordel, at processen er hurtig at starte op, det tager kun 15 minutter, derfor er den mere velegnet til en variabel strømforsyning.
SOEC
Solid Oxide Electrolysis Cell er en nyere teknologi, der ikke rigtigt er slået an endnu. Processen skal køre ved høj temperatur, gerne over 700 grader. Derved bliver strømforbruget væsentligt mindre, tabet forventes at kunne blive bragt ned under 10 %. Til gengæld skal der bruges en del varme, hvorfor SOEC vil være bedst i samspil med en efterfølgende brændstofproduktion, f.eks. ammoniak eller metanol, der begge afgiver betydelige mængder af overskudsvarme.
Princippet i SOEC er vist på fig. 3. Der er ikke nogen vandbeholder men to gitterformede elektroder og en tyk keramisk membran i midten. Vanddamp blæses ind ved katoden, hvor brint skilles fra, mens ilt-ioner passerer gennem membranen og afgiver deres elektroner ved anoden, hvorefter den frie ilt slipper ud.
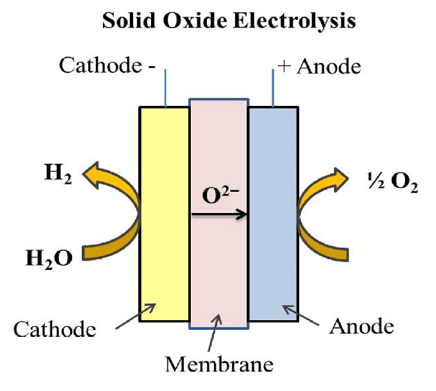
SOEC er stadigvæk på forsøgsstadiet, og det er uvist, hvornår den for alvor kommer i fuld kommerciel drift. De høje driftstemperaturer er en væsentlig komplikation, og materialerne til cellerne er heller ikke billige. Men der er store forhåbninger til teknologien, og bl.a. Haldor Topsøe satser stort på at fremstille keramiske komponenter til den.
Et problem ved SOEC er tilsyneladende stadigvæk en relativt kort levetid for elektroderne og membranen, hvilket vil kræve hyppige, dyre udskiftninger.
SOEC er næppe så velegnet til produktion af brint for sig selv, men derimod er der som nævnt større perspektiver i at kombinere fremstillingen af brint med de næste trin til Power to X.
Vandforbruget
Vandforbruget til elektrolysen er stort, og der er ret skrappe krav til kvaliteten af vandet. Selv grundvand af drikkevandskvalitet kan indeholde for mange salte, der vil forstyrre processen, så ekstra rensning vil være påkrævet. Havvand duer som nævnt slet ikke pga. af klor-indholdet, så det skal afsaltes grundigt inden brugen. Fremstilling af et ton brint kræver knap 10 ton vand, så vandforbruget i processen er noget, der skal tages alvorligt og planlægges omhyggeligt.
Kompressionen
Brint leveret ved atmosfæretryk er frygtelig upraktisk, den fylder alt for meget. Et kg brint vil således fylde ca. 11 kubikmeter. Derfor er det nødvendigt at komprimere brinten til meget højere tryk. Brintbiler har således et tryk i brændstoftanken på 700 bar, for at kunne transportere en rimelig mængde brint på en realistisk plads. Stadigvæk, ved 700 bar, vil en brændstoftank til 5 kg brint fylde ca. 150 liter.
Kompression koster megen energi, som vist på fig. 4. For at bringe brinten op på de 700 bar skal man bruge energi svarende til 6-7 % af brintens energiindhold. Det vil dermed reducere effektiviteten af brintanvendelsen yderligere.
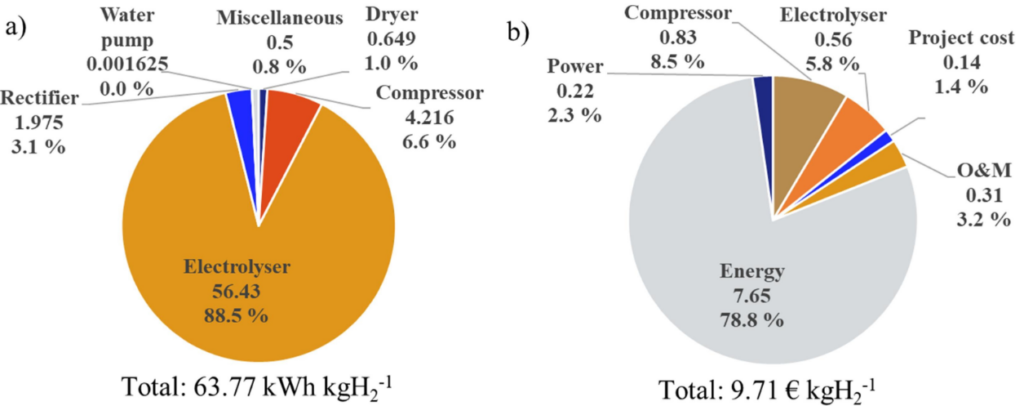
For at hjælpe lidt på situationen er man mange steder overgået til at producere sin brint under tryk. Det kan gøres ganske simpelt ved at indsætte en delvis spærreanordning – en trykregulator – i røret, der fører brinten væk. Elektrolysen leverer brinten under alle omstændigheder, og der er så megen energi i processen, at et tryk op til f.eks. 30 bar kan leveres uden problemer. Man behøver således ikke engang at sætte hele sin alkaliske eller PEM-celle under tryk, der vil så bare være en trykforskel mellem de to halvdele af cellen. Det stiller til gengæld større krav til membranen, da man skal sikre sig at trykket ikke begynder at presse brinten den forkerte vej gennem denne, hvorved brint og ilt vil blive blandet sammen. Alternativt kan man sætte hele cellen under tryk, det kræver så en fødepumpe til vandforsyningen. Dette bliver aktuelt, hvis man ønsker at operere ved meget højere tryk, som også er forsøgt.
Generelt er der ikke vundet noget energimæssigt ved at køre sin elektrolyse under tryk, selv ikke nede omkring de 30 bar. Effektiviteten falder lidt med stigende tryk.
Men princippet har alligevel stor interesse, fordi hvis brinten leveres under tryk, er der meget mindre risiko for, at den forurenes af indsivende luft, og trykket vil også kunne bruges til transport af brinten, f.eks. til den første lagertank.
Sidstnævnte er helt afgørende for ideen om sammenbygning af en vindmølle og et elektrolyseanlæg. Det lyder tosset, men tanken er for så vidt god nok. Vi ved, at vindmøller leverer en højst varierende mængde energi, og den er svær for elforsyningen at håndtere. Jo flere vindmøller, desto større problemer. Hvis f.eks. et Power to X anlæg skal modtage de maksimale mængder af strøm, som vinden kan levere på blæsende dage, skal anlægget være meget stort og vil blive dårligt udnyttet.
Ideen er så, at hver enkelt vindmølle i stedet for at levere elektricitet leverer brint direkte. Møllen skal således udstyres med en elektrolysecelle og forsyning med rent vand, men derefter kan cellen fremstille brint i takt med møllens produktion, og hvis brinten kommer ud med et passende tryk, kan den af sig selv flyde over til en lagertank. Man kunne her forestille sig, at en energiø var udstyret med sådanne lagertanke, og de omkringstående havvindmøller leverede brint til dem. På øen kunne der opstilles en kraftig kompressor til at bringe trykket op, hvorefter brinten kunne pumpes i land til videre brug.
Firmaet Siemens Gamesa har allerede designet sådan en mølle, se fig. 5. Det første eksemplar forventes idriftsat i 2025-2026.
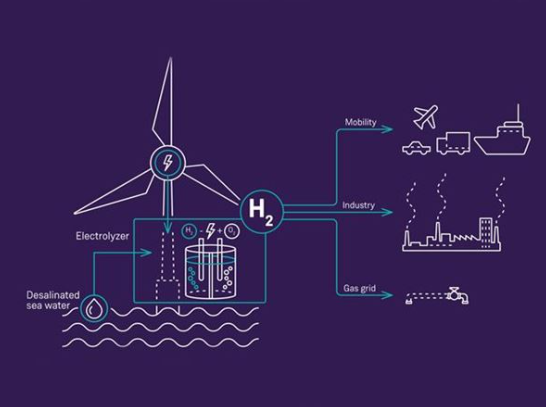
På papiret ser det ud til at være en god idé, men den strider mod det grundlæggende princip inden for al fremstillingsvirksomhed, større volumen giver lavere priser. Med Siemens-møllerne får vi en masse små fabrikker til brint, komplet med egen styring, afsaltning af havvand osv. Tilmed skal alt udstyret opstilles i det værst tænkelige miljø, ved havoverfladen med store mængder af salt i luften, der får alt til at ruste. Reparationer og vedligehold bliver et kapitel for sig, hvor teknikerne skal sejle ud til hver mølle og arbejde med alt udstyret. Det bliver aldrig billigt – og den fremstillede brint vil være endnu mindre konkurrencedygtig på markedet.
I artiklerne i morgen og i overmorgen vil vi kigge nærmere på de konkrete planer i Danmark til fremstilling af brint og Power to X. Hænger det sammen, som initiativtagerne og myndighederne giver udtryk for?








“Haldor Topsøe satser stort på at fremstille keramiske komponenter til den”.. Haldor Topsøe (Nu navngivet Topsoe) udvikler hele elektrolyseanlægget – ikke kun cellen (som rigtignok er keramisk). Første 100 MW anlæg er planlagt i Tyskland.
Det anlæg i Tyskland på 100mw vil jeg rigtig gerne høre mere om, kontakt mig gerne via vi-bygger.dk da jeg ønsker et sådant anlæg på Bornholm 🎐🇩🇰
Venligst Morten Jensen
“Elektrolyse af vand til brint og ilt har været kendt i mere end 200 år. I princippet skal man stikke to elektroder ned i en kop vand og sætte strøm til. Brint vil da boble op ved den ene elektrode og ilt ved den anden, ”
Strøm fra stikkontakten dur ikke. Der kommer både brint og ilt ved begge elektroder.
STRØM skal blot være JÆVNSTRØM eller DC.
Der kommer så Brint ved minus-polen (Katoden).
Firmaet H2Pro er igang med at producere anlæg baseret på en hel ny teknologi de kalder E-TAC.
Det skulle være det mere effektive alternativ til produktion af brint.
E-TAC er en teknologi, der ser lovende ud på papiret og i laboratoriet, men den er formentligt mindst 5-10 år fra at nærme sig noget, der kan bruges i stor skala. Et svagt punkt er helt klart nikkel-hydroxid-elektroden, der skiftevis skal optage OH og derefter afgive ilt og vand. Den virker ikke optimalt uden tilsætning af andre metaller, f.eks. kobolt. Og hvad bliver levetiden af sådan en elektrode, der skal skifte kemi i hver cyklus? Formentligt kort, og hvad koster så udskiftningen?
Jeg ville ikke satse en grøn omstilling på den teknologi.
https://www.nature.com/articles/s41560-019-0462-7.epdf?author_access_token=rI0UIzcWotdOs_GwwDeG7tRgN0jAjWel9jnR3ZoTv0MVEpapPv7W-5kAqqh2YgqlOMFMZXxrNIu9LDZh3CQPITR1rkU16DBZoHbIISRY-rUvgc88FiLOL4xKSyxI6T7yvURm0RKvof2jXeSc3r311Q%3D%3D
Hej Søren
Håber at denne artikel bliver lagret i jeres viden database
En lille trykfejl du skriver at elbiler har en tank med brint, du mener naturligvis brintbiler.
Godt set, tak for det. Er nu rettet.